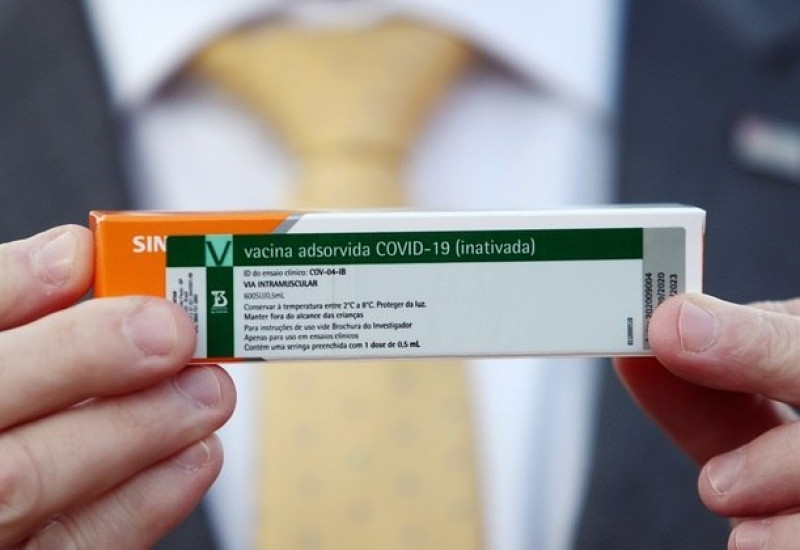
Representantes do
Instituto Butantan e técnicos da Anvisa (Agência Nacional de
Vigilância Sanitária) vão se reunir às 18h desta
quarta-feira (7) para tratar da pré-submissão do pedido de autorização de uso
emergencial da CoronaVac.
Será a segunda
reunião entre eles no dia de hoje. Mais cedo, a agência recebeu dados de eficácia
da fase 3 de testes clínicos, coordenados pelo Butantan com cerca de 12 mil
voluntários no Brasil.
No entanto, ainda
não há definição de o pedido de uso emergencial será formalizado hoje.
As informações
apresentadas pelo Instituto Butantan e pelo governo de São Paulo mais cedo
mostram uma taxa de eficácia de 78% da CoronaVac. Significa que em 100
voluntários vacinados, apenas 22 desenvolveram formas leves da covid-19.
Nenhum caso grave
ou moderado foi registrado, tampouco internações. Os efeitos adversos ocorreram
entre 13% e 38% dos vacinados.
Uma vez oficializada a solicitação de uso emergencial, a Anvisa tem um prazo de até dez dias para dar um parecer. Esta modalidade não permite, por exemplo, a vacinação em massa.
A vacina deve ser
destinada a grupos prioritários específicos, que continuarão sendo monitorados.
O pedido de
registro sanitário da CoronaVac, que é o mais abrangente, ainda não foi feito à
agência. Segundo o diretor do Instituto Butantan, Dimas Covas, isto deve ser
requerido pela Sinovac Biotech, empresa chinesa desenvolvedora do produto após
a consolidação dos dados de outros centros de testes na Turquia e Indonésia,
além da China.
Covas também
afirmou que a CoronaVac é uma das vacinas mais seguras que existem e que cerca
de 700 mil pessoas já receberam esse imunizante na China sem qualquer efeito
adverso significativo.
>>>Clique e receba notícias do JRTV Jornal Regional diariamente em seu WhatsApp.
-
 07/06/2026 - 21h21
07/06/2026 - 21h21 -
 07/06/2026 - 21h12
07/06/2026 - 21h12 -
 07/06/2026 - 20h56
07/06/2026 - 20h56 -
 04/06/2026 - 10h58
04/06/2026 - 10h58 -
 04/06/2026 - 10h29
04/06/2026 - 10h29 -
 04/06/2026 - 10h09
04/06/2026 - 10h09 -
 04/06/2026 - 10h01
04/06/2026 - 10h01
-
 11/05/2020 - 13h19
11/05/2020 - 13h19 -
 03/11/2020 - 22h42
03/11/2020 - 22h42 -
 15/11/2025 - 17h22
15/11/2025 - 17h22 -
 15/12/2021 - 12h59
15/12/2021 - 12h59 -
 10/01/2022 - 14h36
10/01/2022 - 14h36 -
 04/05/2021 - 15h59
04/05/2021 - 15h59 -
 21/01/2022 - 12h23
21/01/2022 - 12h23










DEIXE UM COMENTÁRIO
Facebook