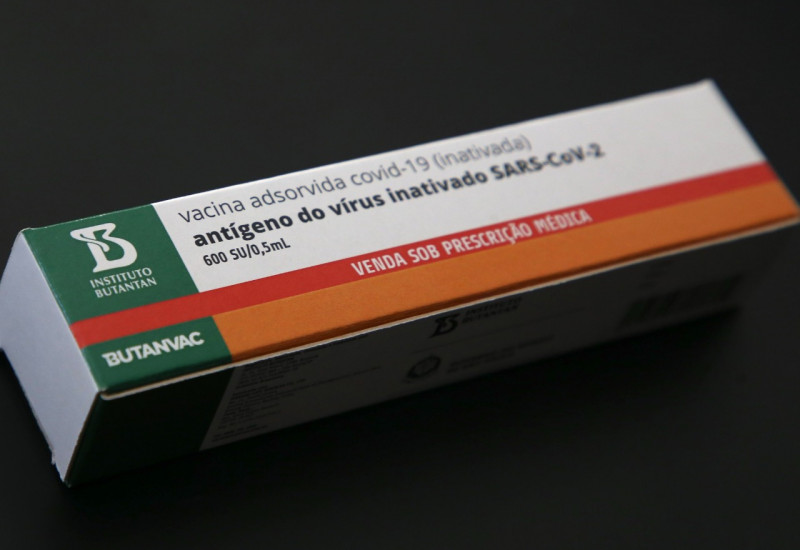
A Anvisa (Agência
Nacional de Vigilância Sanitária) indeferiu o pedido de autorização enviado
pelo Instituto Butantan para dar início à fase de testes em humanos da vacina
desenvolvida pela instituição contra a covid-19, chamada de ButanVac. Segundo a
agência reguladora, os dados enviados pelo Butantan na última sexta-feira (23)
estão “incompletos”.
Veja o comunicado da Anvisa:
Após a análise
técnica dos documentos e informações apresentadas, a Anvisa enviou na
segunda-feira (26/4) para o Instituto Butantan uma exigência com a solicitação
de informações e documentos que ainda não foram apresentados no pedido de
autorização para realização do primeiro estudo clínico em humanos com a
candidata à vacina Butanvac.
Conforme as
regras da Anvisa, o prazo para resposta às exigências é de 120 dias.
O pedido de
autorização do Butantan, enviado à Agência no dia 26/3, e o protocolo do estudo
clínico enviado na última sexta-feira (23/4) ainda estão incompletos e não
atendem aos requisitos técnicos para autorizar pesquisas clínicas de vacinas em
seres humanos.
Com o envio da
exigência, o prazo de análise da Anvisa fica interrompido, já que a Agência
depende das informações do Butantan para dar prosseguimento à análise técnica.
Até o momento, a
candidata a vacina, Butanvac, foi testada apenas em animais.
Dentre os
documentos e informações da proposta de estudo clínico que faltam ser
apresentadas pelo Butantan estão:
– Relatório
técnico contendo dados e informações sobre a caracterização e a definição de
perfil alvo de qualidade da vacina (substância ativa, adjuvantes, interação
ativo + adjuvante e produto terminado).
– Relatório
completo com as informações detalhadas sobre o banco de vírus mestre e de
trabalho (fabricantes, etapas de produção, definição de lotes, controle de qualidade,
estabilidade, lotes utilizados até o momento e lotes a serem utilizados no
estudo clínico).
– Dados e
informações sobre o processo produtivo da vacina (etapas de produção e
parâmetros do processo que podem influenciar nas propriedades estruturais,
físico-químicas e de atividade biológica do antígeno produzido).
– Dados e
Informações sobre o controle de qualidade da vacina (teste de hemaglutinação,
inativação viral, padrão de referência monovalente de vírus, teste de
potência).
– Avaliação de
risco de geração de doença autoimune e necessidade de avaliar a geração de
anticorpos anti DNA por conta de um dos adjuvantes utilizados na vacina.
– Esclarecimento
sobre se os estudos com animais foram realizados com a mesma formulação que
está sendo proposta para teste em seres humanos. Em caso negativo, apresentação
de dados de comparabilidade físico-química entre as formulações da vacina.
– Esclarecimento
sobre o Protocolo Clínico e critérios para escolha de doses e inclusão dos
voluntários.
– Apresentação de
objetivos primários de imunogenicidade e de segurança.
– Cálculo do
tamanho da amostra e métodos estatísticos utilizados.
>>>PARTICIPE DO GRUPO DE NOTÍCIAS NO WHATSAPP.
-
 03/05/2026 - 02h40
03/05/2026 - 02h40 -
 03/05/2026 - 02h08
03/05/2026 - 02h08 -
 03/05/2026 - 02h01
03/05/2026 - 02h01 -
 02/05/2026 - 14h37
02/05/2026 - 14h37 -
 02/05/2026 - 14h19
02/05/2026 - 14h19 -
 02/05/2026 - 13h44
02/05/2026 - 13h44 -
 01/05/2026 - 13h29
01/05/2026 - 13h29
-
 11/05/2020 - 13h19
11/05/2020 - 13h19 -
 03/11/2020 - 22h42
03/11/2020 - 22h42 -
 15/11/2025 - 17h22
15/11/2025 - 17h22 -
 15/12/2021 - 12h59
15/12/2021 - 12h59 -
 10/01/2022 - 14h36
10/01/2022 - 14h36 -
 04/05/2021 - 15h59
04/05/2021 - 15h59 -
 21/01/2022 - 12h23
21/01/2022 - 12h23










DEIXE UM COMENTÁRIO
Facebook