No final da tarde
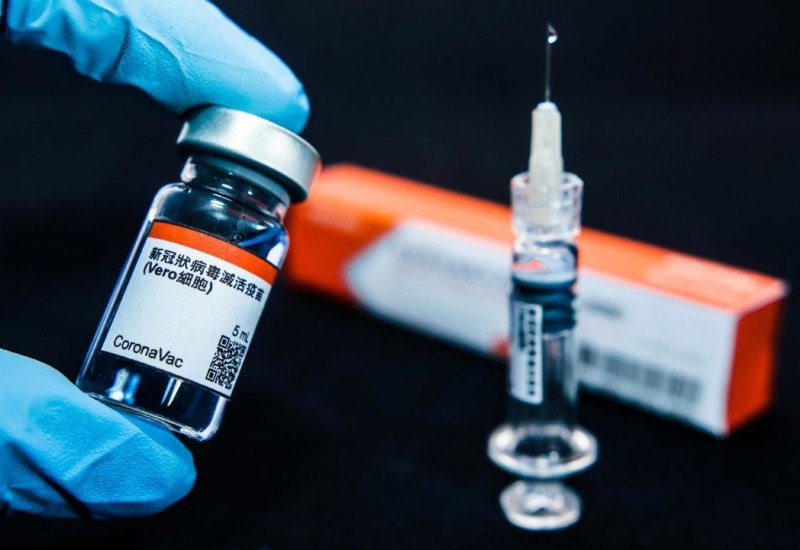
desta sexta-feira (23) a Agência Nacional de Vigilância Sanitária (Anvisa)
autorizou a importação de 6 milhões de doses da vacina chinesa contra a
Covid-19 desenvolvida pelo laboratório Sinovac.
Essa aquisição está
relacionada com o programa de imunização da doença desenvolvido pelo Instituto
Butantan, em São Paulo. Até o fim do ano, o instituto espera produzir outras 40
milhões de doses — essas 6 milhões primeiras serão 100% produzidas na China. O
que sobrar deverá ser produzido a partir do princípio ativo importado.
O governador João
Doria e as autoridades do estado de São Paulo já foram informados dessa
aquisição.
A Anvisa afirmou
ainda nesta sexta, através de uma nota que “não há nenhum tipo de retardo,
atraso ou morosidade” diante do pedido do Instituto Butantan. A Anvisa está
colocando o pedido de importação de vacinas já envasadas do Instituto Butantan
sob análise da ferramenta eletrônica formal, chamada circuito deliberativo, na
qual os diretores podem analisar o processo e efetuar a votação sem a
necessidade das formalidades de uma reunião presencial e pública da Diretoria
Colegiada”, dizia o documento encaminhado à imprensa.
A Anvisa enviou uma
nota afirmando que:
“A Anvisa
autorizou nesta sexta-feira (23/10) a importação de 6 milhões de doses da
Vacina Adsorvida Covid-19 (inativa), fabricada por Sinovac Life Sciences Co.
LTD. A solicitação foi feita pelo Instituto Butantã para importação, em caráter
excepcional, de vacina adsorvida covid-19 (inativa), em estudo clínico fase
III, ainda sem registro no Brasil. O tema foi discutido em Circuito
Deliberativo, entre esta quinta e sexta-feira (22-23/10). O Circuito
Deliberativo é uma instância de votação online dos diretores da Agência. A
autorização contempla o regramento de importação.
Por oportuno,
necessário esclarecer que a carga ficará sob a guarda do Instituto Butantan,
seu fiel depositário, mediante termo de guarda específico pertinente, que
deverá mantê-la em suas instalações e em perfeitas condições de
acondicionamento, até que seja autorizada a utilização
Na importação em
caráter excepcional de produto sem registro, é de responsabilidade do
importador garantir a eficácia, segurança e qualidade do produto, inclusive o
monitoramento do seu uso e o exercício da farmacovigilância. Adicionalmente, a
utilização do produto ficará condicionada à obtenção de seu registro sanitário
junto à Anvisa”
>>>Clique e receba notícias do JRTV Jornal Regional diariamente em seu WhatsApp.
-
 07/06/2026 - 21h21
07/06/2026 - 21h21 -
 07/06/2026 - 21h12
07/06/2026 - 21h12 -
 07/06/2026 - 20h56
07/06/2026 - 20h56 -
 04/06/2026 - 10h58
04/06/2026 - 10h58 -
 04/06/2026 - 10h29
04/06/2026 - 10h29 -
 04/06/2026 - 10h09
04/06/2026 - 10h09 -
 04/06/2026 - 10h01
04/06/2026 - 10h01
-
 11/05/2020 - 13h19
11/05/2020 - 13h19 -
 03/11/2020 - 22h42
03/11/2020 - 22h42 -
 15/11/2025 - 17h22
15/11/2025 - 17h22 -
 15/12/2021 - 12h59
15/12/2021 - 12h59 -
 10/01/2022 - 14h36
10/01/2022 - 14h36 -
 04/05/2021 - 15h59
04/05/2021 - 15h59 -
 21/01/2022 - 12h23
21/01/2022 - 12h23










DEIXE UM COMENTÁRIO
Facebook